جمعه, ۳۱ فروردین, ۱۴۰۳ / 19 April, 2024
مجله ویستا
مروری جامع بر خصوصیات ویروس بیماری برونشیت عفونی

طبیعت بالای انتقال این بیماری و وقوع چندگانه سروتیپهای ویروس این بیماری ( IBV ) حالت بسیار پیچیده ایی را ایجاد کرده و توجه تولیدکنندگان را در جهت پیشگیری از بروز این بیماری افزایش میدهد . اما بایستی توجه داشت که بروز بیماری برونشیت عفونی ، سبب صدمه خوردن به سلامت عمومی جامعه نخواهد شد .
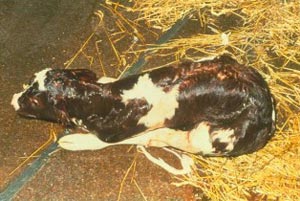
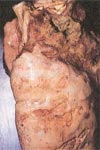
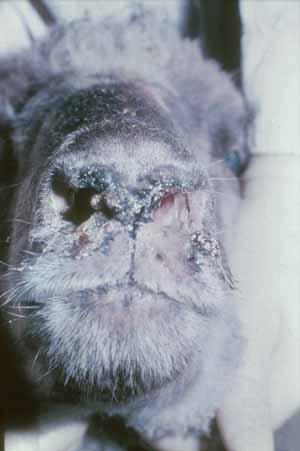
زیانهای مالی ناشی از بروز برونشیت ، معمولا بدلیل کاهش تولید میباشد و نه مرگ و میر . اگرچه در جوجه های گوشتی ، مرگ و میر از درجه اهمیت بالایی برخوردار میباشد . میزان مرگ و میر در جوجه های گوشتی ظرف مدت دو هفته به حداکثر مقدار ممکن می رسد . این واقعه نیز در سن پنج تا شش هفتگی زندگی آنها روی میدهد . مرگ و میر نیز بطور معمول بر اثر عفونتهای باکتریایی ثانویه روی میدهد . عفونتهای باکتریایی نیز بدلیل صدمه خوردن به مجاری تنفسی بر اثر ویروس بیماری برونشیت ( IBV ) میباشد .
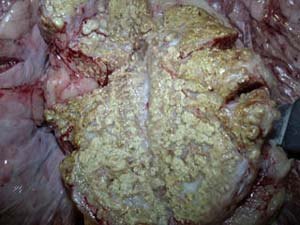
برخی از زنجیره های این ویروس ، بشدت خاصیت Nephropathogenic داشته و توانایی گرفتن تلفات تا ۳۰ درصدی را از گله های جوجه های جوان دارند .
ویروس این بیماری در داخل Oviduct نیز تکثیر می یابد . بیماری برونشیت عفونی در پرندگانی که سن بالا دارند میتوانند منجر به کاهش ۱۰ تا ۵۰ درصدی و یا بیشتر در تولید میشود . همچنین با بروز این بیماری ، تولید تخم مرغهای بدشکل نیز افزایش خواهند یافت . بطور معمول ، میزان تولید ، پس از بروز این بیماری به حالت عادی باز نخواهد گشت . برخی از مواقع ، بروز این بیماری در پرندگان جوان ، سبب رشد ناقص و ناکافی Oviduct خواهد شد .
انواعی از خانواده CoronaVirus که شباهتهای ژنی زیادی را با IBV دارند ، از قرقاول ها و بوقلمونها جدا شده اند . اما انواعی از CoronaVirus هایی که در اینگونه پرندگان دیده میشوند ، بایستی بصورت جداگانه و در مبحثی دیگر بررسی شوند .
● تاریخچه
بیماری برونشیت عفونی برای نخستین بار در سال ۱۹۳۰ در Dakota شمالی در ایالات متحده آمریکا مشاهده شد . در سال ۱۹۳۱ ، Hawn و Schalk گزارشی را مبنی بر مطالعه و همچنین بررسی کلینیکی و آزمایشگاهی این بیماری منتشر کرده اند که میتوان آن را نخستین مورد بررسی این بیماری دانست .
در ابتدا ، IB بعنوان نوعی بیماری مخصوص پرندگان جوان شناخته شد . بهرحال ، پس از گذشت مدت زمانی ، این بیماری در طیور با سن بالاتر و همچنین طیور تخمگذار نیز دیده شد . سایر نشانه های ثبت شده شامل : علائم تنفسی در سال ۱۹۴۰ و ضایعاتی در کلیه در سال ۱۹۶۰ بوده است .
اهمیت اقتصادی شیوع این بیماری در گله های طیور پرورشی ، سبب شد تا اقداماتی در جهت جلوگیری از بروز این بیماری در دوره های رشد و همچنین تولید تخم مرغ در نظر گرفته شود . این دسته از اقدامات ، توسط VanRokel در سال ۱۹۴۱ صورت گرفت که با برخی موفقیتها نیز همراه شد . این دسته از اقدامات را میتوان ، نخستین قدم به سوی شکل گیری اقدامات پیشگیرانه امروزی دانست .
از نقاط عطف دیگری که میتوان به آنها اشاره نمود ، شناخت اتیولوژی این ویروس در سال ۱۹۳۶ توسط Beach و Schalm بود . همچنین نخستین کشت ویروس در جنین مرغ ( داخل تخم مرغ ) توسط Beaudette و Hudson در سال ۱۹۳۷ صورت گرفت .
در سال ۱۹۵۶ ، گزارشی توسط Jungherr و Colleagues منتشر شد مبنی بر جداسازی Connecticutt . در سالهای ۱۹۴۱ و ۱۹۵۱ نیز گزارشهایی مبنی بر جداسازی سویه Massachusetts ثبت شده است .
برای نخستین بار گزارشی از سوی Jungherr منتشر شد . با انتشار این گزارش ، مشخص شد که اتیولوژی IB شامل بیش از یک نوع سروتایپ میباشد . سایر مطالعات اولیه در مورد این بیماری توسط Fabri Caul صورت گرفت .
● شیوع و گسترش
بیماری برونشیت عفونی در سراسر دنیا گسترش یافته است . در ایالات متحده ، علاوه بر سویه های بومی ( نوع Massachusetts یا Mass ) چندین سروتایپ دیگر نیز شناخته شده است . در ابتدای سال ۱۹۵۰ میلادی ، زنجیره های نوع Mass در اروپا مشاهده شدند . در واقع ، بسیاری از انواع سروتیپهایی که در آمریکای شمالی شناسایی شده بودند ، پس از مدتی در آفریقا نیز مشاهده شدند . این بیماری در کشورهای آسیایی چون هند ، ژاپن ، کره و چین و همچنین استرالیا و اروپا شیوع یافته است .
غالبا شیوع IB حتی در گله های واکسینه شده نیز روی میدهد . انواع ویروسهای جدا شده از این دسته شیوع ، غالبا ( نه همیشه ) از سروتایپی متمایز از واکسن میباشند .
▪ اتیولوژی
طبقه بندی :
ویروس بیماری برونشیت عفونی از خانواده Coronaviridae میباشد . این ویروس شامل دو جنس میباشد :
۱) Coronavirus .
۲) Torovirus .
در واقع ، IBV عضو گروه سوم جنس Coronavirus میباشد . دو گروه دیگر شامل انواع Coronavirus موجود در پستانداران میباشد که بطور گسترده ایی از لحاظ سازمان یافتگی ژنوم و تناوب ژنی با ویروس برونشیت عفونی متفاوت است . طبق گزارشات ارائه شده ، بیان نحوه مصونیت انسان در برابر این بیماری بسیار مشکل است .
اخیرا نشان داده شده است که برخی از انواع Coronavirus های جدا شده از بوقلمونها شباهت بسیار زیادی به IBV دارند . این ویروسها ، نیز در گروه سوم Coronavirus ها طبقه بندی میشوند . تاکنون بطور قطعی انواعی از Torovirus ها بعنوان عامل بیماریزا در پرندگان شناسایی نشده است .
▪ مورفولوژی
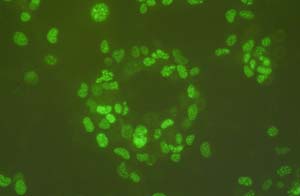
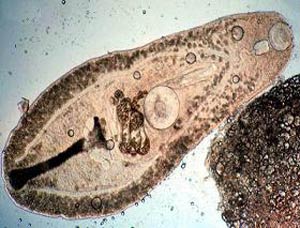
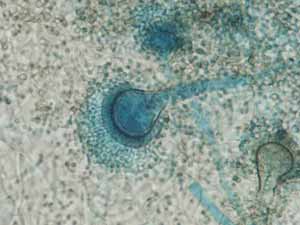
ویروس بیماری برونشیت عفونی از لحاظ شکلی بسیار پلئومورفیک ( Pleomorphic ) است . با تحقیقات صورت گرفته و همچنین آنالیزهای انجام شده ، مشخص شده است که این ویروس ۱۲۰ نانومتر قطر و ۲۰ نانومتر طول دارد . در سطح این ویروس نیز زائده های گرز مانندی وجود دارد . بایستی توجه داشت که این زائده ها همانند گروه ParamyxoVirus نمیباشد . در این گروه ، زائده های از یکدیگر فاصله دارند اما در گروه ParamyxoVirus ، این زائده ها با فاصله بسیار کمی از یکدیگر قرار گرفته اند .
ساختمان رینوکلئوپروتئینها ( RNP ) در اینحالت بصورت قطعه قطعه شده دیده میشود . توجه داشته باشید که این ذرات را با آلودگیها اشتباه نگیرید . در اکثر نمونه ها ، قطر RNP بصورت استاندارد ، یک تا دو میلیمتر در نظر گرفته میشود . اما در برخی از مشاهدات ، بصورت اتفاقی ذراتی با ساختمان حلقوی و قطر ۱۰ تا ۱۵ نانومتری گزارش شده است . اگرچه تاکنون نوع ToroVirus در این بیماری مشاهده نشده است ، گزارشهای ثبت شده ، حاکی از شباهت بسیار بالای ToroVirus و CoronaVirus در میکروسکوپ الکترونی میباشد .
گونه های مختلف ویروس برونشیت عفونی ، در فشردگی دانه های ساکاروز با یکدیگر متفاوت میباشند . از سوی دیگر ، سانتریفیوژ با قدرت بیشتر از ۱۰۰.۰۰۰ دور سبب از بین رفتن گرزها و قسمتهای مختلف این ویروس میشود . با تحقیقات صورت گرفته ، زیرمجموعه های S۱ بعنوان عوامل فرم گرفتن پروتئینهای قسمتهای گرز مانند شناخته شده اند . انکوباسیون ویروس در دمای ۳۷ درجه سانتی گراد میتواند نجر به از بین رفتن زیرمجموعه های S۱ شود .
● ترکیب شیمیایی
ویروس بیماری برونشیت عفونی ، شامل سه ساختمان پروتئینی مهم میباشد :
۱) زائده های میخ مانند ( S ) .
۲) غشاء ( M ) .
۳) گلیکوپروتئینها و نوکلئوپروتئینها ( N ) .
بعلاوه ، پروتئین چهارم ( CE ) بعنوان عامل تشکیل دهنده پوشش ویروس شناخته شده است .
پروتئین S ، دو تا سه کپی را ار هریک از دو گلیکوپپتیدها میگیرد ( S۱ و S۲ ) . این پروتئینها به ترتیب واجد ۵۲۰ و ۶۲۵ آمینواسید میباشند . آزمایشاتی چون HI (Hemagglutination Inhibiting ) و همچنین روش خنثی سازی ویروس ( VN ) بر پایه پروتئینهای S۱ میباشند .
تنها در حدود ۱۰ درصد از پروتئینهای M ، بدون حفاظ و در سطوح خارجی ویروس قرار دارند . پروتئین N نیز در اطراف بخش Single Stamdard قرار دارد . ژنوم RNA ویروس ( فرم RNP ) نهایتا از ۲۷۶۰۰ نوکلئوتید تشکیل شده است که هرکدام از آنها کلون شده و متناوب میباشند . پاکسازی و تصویه ویروس در سلولهای پلی پپتید میزبان صورت می گیرد . تشخیص پروتئین S۲ از طریق روش Coomassic Blue Staining مشکل بوده و برخی از پروتئینهای N نیز تجزیه شده و از بین میروند .●تکثیر ویروس
ویروس بیماری برونشیت عفونی ( IBV ) در سیتوپلاسم تکثیر میشود . در یک مکانیسم نسخه برداری غیر ادامه دار ، شش RNA پیام رسان ترکیبی دوباره را پدید می آورند . ترکیب ویروس نیز ، با انجام عملیاتی در غشاء آندوپلاسمیک رتیکولوم روی میدهد و نه در سطوح سلول .
پروتئینهای S بر خلاف پروتئینهای M ، در میان رتیکولوم ( Reaticulum ) به سطوح سلول مهاجرت می کنند . ویروسهای جدید ظرف مدت سه تا چهار ساعت پس از آلودگی شروع به پیدایش می کنند . ظرف مدت ۱۲ ساعت ، در ۳۷ درجه سانتیگراد تعداد زیادی از این ویروسها پدید می آیند .
● مقاومت به عوامل شیمیایی و فیزیکی
بیشتر گونه های IBV پس از ۱۵ دقیقه در ۵۶ درجه سانتیگراد و یا پس از ۹۰ دقیقه در ۴۵ درجه سانتیگراد غیرفعال میشوند . بایستی توجه داشت که ذخیره IBV در ۲۰ درجه سانتی گراد نیز اشتباه است . اگرچه عفونت مایع آلانتوئیک پس از ذخیره سازی در ۳۰ درجه سانتی گراد ، سالهای زیادی زنده خواهد ماند . بافتهای آلوده ذخیره شده در گلیسرول ۵۰ درصد بخوبی حفظ شده و این بافتها را میتوان به این وسیله و بدون قرار گیری در یخچال به آزمایشگاه ارسال نمود . بقای این ویروس در هوای آزاد ، در بهار تا بالای ۱۲ روز و در زمستان تا ۵۶ روز گزارش شده است .
● لئوفیلیزه سازی
مایع آلانتوئیک عفونی لئوفیلیزه شده ، سفت شده تحت فشار و نگاه داشته شده در یخچال برای حداقل ۳۰ سال قابل استفاده خواهد بود . در شرایطی که IBV ، لئوفیلیزه شده و منجمد شده است گلوکز ۱۰ درصد اثر تثبیت کننده به آن می دهد .
● ثبات و پایداری در PH های مختلف
تاکنون سه گزارش مختلف با توجه به ثبات ویروس این بیماری در PH های مختلف منتشر شده است . در یکی از بررسیهای صورت گرفته با قرار گرفتن ویروس این بیماری در دمای اطاق در معرض PH ، ۳ برای مدت زمان ۴ ساعت کاهش تیتر log۱۰ ۲ – ۱ تا log۱۰ ۵ مشاهده شد . در بررسی دیگری مشخص گردیده است که پایداری این ویروس در محیط سلول در PH متوسط ( ۶ تا ۶.۵ ) بیشتر از PH ۷ تا ۸ بوده است .
● عوامل شیمیایی
بطور معمول ، IBV به اتر حساس است . اما برخی از گونه های این ویروس در اتر ۲۰ درصد زنده خواهند ماند ( ۴ درجه سانتی گراد ، هجده ساعت ) . از سوی دیگر ، ویروس این بیماری با کلروفرم ۵۰ درصد ( دمای اطاق ، ۱۰ دقیقه ) و ۰.۱ درصد Sodium Deoxycholate ( ۴ درجه سانتی گراد ، ۱۸ ساعت ) نابود میشود .
حساسیت ویروس این بیماری به مواد ضدعفونی کننده معمولی را در بسیاری از مطالعات بررسی کرده اند . غلظت ۰.۰۵ تا ۰.۱ درصد Beta Propiolactone ( BPL ) یا ۰.۱ درصد فرمالین فعالیت IBV را متوقف می کند . از سوی دیگر ، تنها استفاده از BPL هیچگونه تاثیر جانبی را بر روی فعالیت Hemagglutination آنتی ژن ویروس برونشیت عفونی نخواهد گذاشت .
● طبقه بندی گونه
طبقه بندی گونه و همچنین ژنوتیپ IBV بر اساس مشخصه پروتئین S میباشد . راههای زیادی برای تمایز و جداسازی IBV وجود دارد . این راهها را De Wit پیشنهاد داده است . تاکنون ۱۲ سروتیپ مختلف از IBV شناسایی شده است . البته بدون شک ، این تعداد بسیار بیشتر خواهد بود .
بصورت مرسوم ، سروتیپهای IBV بوسیله آزمایش VN AntiBody شناخته میشوند . در این روش از زیرمجموعه S۱ پروتئین S استفاده میشود . آزمایش VN به زمان حساسیت زیادی دارد . با افزایش تعداد سروتیپهای استاندارد ، این حساسیت از درجه اهمیت بالایی برخوردار است . در حال حاضر ، بسیاری از آزمایشگاهها از آنتی بادیهای Mono Clonal استفاده می کنند . این آنتی بادی ها به مخصوص سروتیپهای مشخص میباشند . ایندسته از آنتی بادیها در آزمایش ELISA ( Enzyme Linked Immunosorbent Assays ) استفاده میشوند . این آزمایش بصورت فزاینده ایی در آزمایشگاه ها انجام میشود و باصرفه تر از روش VN میباشد .
در خلال عفونتهای چندگانه ، امکان خواهد داشت که IBV تحت ترکیبی دوباره قرار گیرد . البته این نکته را در ذهن داشته باشید که سروتایپهای این ویروس در گروههای مشخصی طبقه بندی شده اند . Corona Virus های جداشده از بوقلمونها و همچنین قرقاولهای پرورشی در ایالات متحده ، از نظر ترتیب ژنی بررسی شده اند . ایندسته از ویروسها بطور شفاف به ویروس بیماری برونشیت عفونی ( IBV ) شباهت زیادی دارند ( بطور مثال ، انواع Corona Virus هایی که آنها را میتوان در پرندگان وحشی یافت ) .
● بررسی آنتی بادی سرم
بین سالهای ۱۹۶۰ تا ۱۹۷۰ چندین گونه متمایز از هم در گروههای مشخصی در آمریکا و استرالیا تعریف شدند . پس از آن بسیاری از گونه های جدید IBV در آسیا و اروپا شناخته شدند .
بی اثرسازی ویروس با استفاده از ارگانهای تنفسی طبیعی ( TOC&#۰۳۹;S ) صورت گرفته است . سلولهای کلیه مرغها ( CK ) نیز توانایی کاهش پلاک را دارند . در واقع ، آزمایشات متقاطع خنثی سازی در مورد بسیاری از گونه های جداشده در Arkansas ( Ark ) سبب پدید آمدن برخی از دسته بندیهای جدید شد .
امکان طبقه بندی گونه ها ( SeroTyping ) از طریق آزمایش HI نیز بررسی شده است . در آزمایش HI ، پاسخ آنتی بادی بدنبال نوعی در معرض قرارگیری منفرد بوده و بنابراین نتیجه آن نیز بسیار اختصاصی میباشد . نمونه آن نیز تمایز گونه M۴۱ از گونه Mass میباشد .
علت استفاده از آزمایش HI در Serotyping را میتوان تخصصی بودن پاسخهای اولیه و همچنین محدودیت در ایجاد واکنشهای متقاطع دانست . از سوی دیگر ، Cook et al ، آزمایش HI را با آزمایش VN از طریق TOC بررسی کرده و گزارشی را مبنی بر وجود واکنشهای متقاطع فراوان در آزمایش HI منتشر ساختند و بیان نمودند که گونه های مختلف IBV با استفاده از آزمایش VN بخوبی از یکدیگر متمایز خواهند شد . در این مطالعه مبنای کار ، ارزیابی نتایج اولیه بود . دلیل اینکار نیز ، واکنش پذیری اغلب نتایج ثانویه میباشد . لازم بذکر است که بایستی IBV را با استفاده از فراورده های آنزیمی و اجزای فعال تهیه نمود تا قابل استفاده در مرحله HA باشد .
● بررسی آنتی بادیهای MonoClonal
آنتی بادیهای منوکلونال در گونه های مختلفی از آمریکا همچون ماساچوست ، Connecticut ۴۶ و Arkansas ۹۹ گسترش یافته اند . این وضعیت در گروههای اروپایی چون D۲۴۷ ، D۱۴۶۶ و همچنین گونه های جداشده در استرالیا نیز دیده میشود . این نوع آنتی بادیها جهت تمایز گونه های مختلف IBV مفید بوده و فعالیت آنها برعلیه زیررده های خوشه های پروتئین S۱ میباشد . گروههای آنتی ژنیک استرالیایی که از طریق ایندسته از آنتی بادی ها جدا شده اند همبستگی بهتری با یکدیگر دارند .
● بررسی اسیدهای نوکلوئیک
توالی های ژنوم گونه Beaudette و همچنین بسیاری از گونه های مختلف IBV تاکنون شناسایی شده است . با بررسیهای صورت گرفته مشخص شده است ژنی که در اغلب موارد توالی یافته است ، نوعی است که در زیرگروه خوشه گلیکوپروتئینی S۱ کد شده است . از سوی دیگر ، پروتئین S۱ نقش مهمی را در ایجاد ایمنی حفاظتی بازی میکند .
از این گذشته ، تغییرات بزرگی که در برخی از توالی ها روی میدهد و پروتئین S۱ مسئول آنها میباشد ، سبب تکثیر برخی از گونه های مختلف ویروس شده و باعث بروز بیماری میشوند . بروز بیماری در حالی صورت میگیرد که سایر گونه ها سبب بروز برخی از پاسخهای ایمنی در بدن شده اند .
بسیاری از زیرگروههای توالی ژنی پروتئین S۱ ، اشاعه یافته و در بانک اطلاعاتی نوکلئوتید جایگزین شده است .
تهیه ، تنظیم و ترجمه :
علیرضا گائینی . دانشجوی رشته دکترای دامپزشکی . دانشگاه آزاد اسلامی واحد گرمسار .
منبع :Disease Of Poultry . ۱۱Th Edition
علیرضا گائینی . دانشجوی رشته دکترای دامپزشکی . دانشگاه آزاد اسلامی واحد گرمسار .
منبع :Disease Of Poultry . ۱۱Th Edition
منبع : موسسه مرغداری ایران
همچنین مشاهده کنید
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
خرید میز و صندلی اداری
خرید بلیط هواپیما
گیت کنترل تردد
اسرائیل ایران حمله ایران به اسرائیل آمریکا گشت ارشاد ایران و اسرائیل ارتش جمهوری اسلامی ایران دولت دولت سیزدهم وعده صادق جنگ جنگ ایران و اسرائیل
سیل قتل قوه قضاییه هواشناسی تهران کنکور سیلاب شهرداری تهران آموزش و پرورش پلیس سازمان هواشناسی فضای مجازی
قیمت خودرو خودرو قیمت دلار قیمت طلا تورم بازار خودرو ایران خودرو بانک مرکزی حقوق بازنشستگان بورس دلار قیمت سکه
تلویزیون احسان علیخانی ازدواج سینمای ایران تبلیغات شبکه نمایش خانگی کتاب موسیقی دفاع مقدس سریال تئاتر سینما
دانشگاه تهران دانشگاه آزاد اسلامی
رژیم صهیونیستی عملیات وعده صادق غزه فلسطین جنگ غزه روسیه چین حماس سازمان ملل اسراییل طوفان الاقصی لبنان
پرسپولیس فوتبال صنعت نفت آبادان لیگ قهرمانان اروپا رئال مادرید استقلال بارسلونا بازی لیگ برتر کشتی فرنگی تراکتور سپاهان
هوش مصنوعی سامسونگ تلگرام اپل وزیر ارتباطات ایلان ماسک ناسا عیسی زارع پور
سلامت پزشک چاقی پیاده روی درمان و آموزش پزشکی دیابت سلامت روان