چهارشنبه, ۵ اردیبهشت, ۱۴۰۳ / 24 April, 2024
مجله ویستا
پایداری و ناپایداری
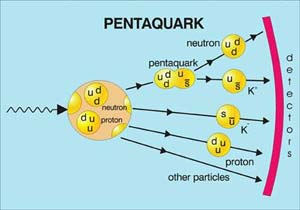
اگر ۱۳ پروتون را با ۱۴ نوترون ترکیب کنیم هستهای خواهیم داشت که اگر ۱۳ الکترون در اطراف آن گردش کنند یک اتم آلومینیوم را میسازند. حال اگر میلیاردها از این اتمها را در کنار هم قرار دهیم فلز آلومینیوم (AL۲۷) را داریم که با آن انواع وسایل نظیر قوطی نوشابه و درب و پنجره و غیره... را میتوان ساخت. اگر همین آلومینیوم را در شیشهای قرار دهیم و چند میلیون سال دیگر به سراغ آن بیائیم این آلومینیوم هیچ تغییری نخواهد داشت. یعنی آلومینیوم عنصری پایدار است. تا حدود یک قرن پیش تصور بر این بود که تمام عناصر پایدار هستند. بسیاری از اتمها در اشکال متفاوتی دیده می شوند. برای مثال مس دو شکل پایدار دارد: مس ۶۳ ومس ۶۵ . به این دو نوع ایزوتوپ گفته می شود. هر دوی آنها ۲۹ پروتون دارند اما چون در عدد اتمی ۲ واحد فرق دارند به سادگی می توان فهمید که تعداد نوترون های اولی ۳۴ ودیگری ۳۶ است. هر دوی آنها پایدار هستند. در حدود یک قرن پیش دانشمندان متوجه شدند گه همه عناصر ایزوتوپهایی دارند که رادیواکتیو (پرتوزا) هستند. مثلا هیدروژن را در نظر بگیرید، در مورد این عنصر سه ایزوتوپ شناخته شده است:
۱ - هیدروژن معمولی (H۱) در هسته اتم حود یک پروتون دارد وبدون هیچ نوترونی. البته واضح است چون نیازی نیست تا خاصیت چسبانندگی خود را نشان دهد چرا که پروتون دیگری وجود ندارد.
۲ - هیدروژن دوتریم که یک پروتون ویک نوترون دارد و در طبیعت بسیار نادر است. اگرچه عمل آن بسیار شبیه هیدروژن نوع اول است برای مثال میتوان از آن آب ساخت اما میزان بالای آن سمی است. هر دو ایزوتوپ یاد شده پایدار هستند اما ایزوتوپ دیگری از هیدروژن وجود دارد که ناپایدار است!
۳ - ایزوتوپ سوم هیدروژن (تریتیوم) که شامل دو نوترون و یک پروتون است. همان طور که قبلا گفته شد این نوع هیدروژن ناپایدار است . یعنی اگر بازهم ظرفی برداریم واین بار درون آن را با این نوع از هیدروژن پر کنیم و یک میلیون سال دیگر به سراغ آن بیائیم متوجه میشویم که دیگر هیدروژنی نداریم و همه آن به هلیم ۳ تبدیل شده است (۲ پروتون و یک نوترون). میتوان گفت که هر چه هسته اتم سنگینتر شود تعداد ایزوتوپها بیشتر میشود و هر چه تعداد ایزوتوپها بیشتر شود امکان بوجود آمدن هستههای ناپایدار نیز بیشتر خواهد شد و در نتیجه احتمال وجود نوع رادیواکتیو نیز بیشتر میشود. در طبیعت عناصر خاصی را میتوان یافت که همه ایزوتوپهایشان رادیواکتیو باشند. برای مثال دو عنصر سنگین طبیعت که در بمبها ونیروگاههای هستهای از آنها استفاده می شود را نام میبریم: اورانیوم و پلوتونیوم.
خصوصیات فیزیکی اورانیوم:
اورانیوم طبیعی (که بهشکل اکسید اورانیوم است) شامل۳/۹۹% از ایزوتوپ اورانیوم ۲۳۸ و۷/۰% اورانیوم ۲۳۵است. که نوع ۲۳۵ آن قابل شکافت است و مناسب برای بمبها ونیروگاههای هستهای است. این عنصر از نظر فراوانی در میان عناصر طبیعی پوسته زمین در رده ۴۸ قراردارد. از نظر تراکم و چگالی باید گفت ۶/۱ مرتبه متراکم تر از سرب است. همین تراکم باعث سنگینتر شدن آن میشود. برای مثال اگر یک گالن شیر وزنی حدود چهار کیلوگرم داشته باشد ,یک گالن اورانیوم ۷۵ کیلوگرم وزن دارد.
انواع اورانیوم:
اورانیوم با غنای پایین که میزان اورانیوم ۲۳۵ آن کمتر از ۲۵% ولی بیشتر از۷/۰% است که سوخت بیشتر راکتورهای تجاری بین ۳ تا ۵ درصد اورانیوم ۲۳۵ است. اورانیوم با غنای بالا که در فرآیند غنیسازی اورانیوم تهیه میشود. اورانیوم ۲۳۵ در آن بیشتر از ۲۵% وحتی در مواردی تا ۹۸% است و مناسب برای کاربردهای نظامی وساخت بمبهای هستهای است.
۱ - هیدروژن معمولی (H۱) در هسته اتم حود یک پروتون دارد وبدون هیچ نوترونی. البته واضح است چون نیازی نیست تا خاصیت چسبانندگی خود را نشان دهد چرا که پروتون دیگری وجود ندارد.
۲ - هیدروژن دوتریم که یک پروتون ویک نوترون دارد و در طبیعت بسیار نادر است. اگرچه عمل آن بسیار شبیه هیدروژن نوع اول است برای مثال میتوان از آن آب ساخت اما میزان بالای آن سمی است. هر دو ایزوتوپ یاد شده پایدار هستند اما ایزوتوپ دیگری از هیدروژن وجود دارد که ناپایدار است!
۳ - ایزوتوپ سوم هیدروژن (تریتیوم) که شامل دو نوترون و یک پروتون است. همان طور که قبلا گفته شد این نوع هیدروژن ناپایدار است . یعنی اگر بازهم ظرفی برداریم واین بار درون آن را با این نوع از هیدروژن پر کنیم و یک میلیون سال دیگر به سراغ آن بیائیم متوجه میشویم که دیگر هیدروژنی نداریم و همه آن به هلیم ۳ تبدیل شده است (۲ پروتون و یک نوترون). میتوان گفت که هر چه هسته اتم سنگینتر شود تعداد ایزوتوپها بیشتر میشود و هر چه تعداد ایزوتوپها بیشتر شود امکان بوجود آمدن هستههای ناپایدار نیز بیشتر خواهد شد و در نتیجه احتمال وجود نوع رادیواکتیو نیز بیشتر میشود. در طبیعت عناصر خاصی را میتوان یافت که همه ایزوتوپهایشان رادیواکتیو باشند. برای مثال دو عنصر سنگین طبیعت که در بمبها ونیروگاههای هستهای از آنها استفاده می شود را نام میبریم: اورانیوم و پلوتونیوم.
خصوصیات فیزیکی اورانیوم:
اورانیوم طبیعی (که بهشکل اکسید اورانیوم است) شامل۳/۹۹% از ایزوتوپ اورانیوم ۲۳۸ و۷/۰% اورانیوم ۲۳۵است. که نوع ۲۳۵ آن قابل شکافت است و مناسب برای بمبها ونیروگاههای هستهای است. این عنصر از نظر فراوانی در میان عناصر طبیعی پوسته زمین در رده ۴۸ قراردارد. از نظر تراکم و چگالی باید گفت ۶/۱ مرتبه متراکم تر از سرب است. همین تراکم باعث سنگینتر شدن آن میشود. برای مثال اگر یک گالن شیر وزنی حدود چهار کیلوگرم داشته باشد ,یک گالن اورانیوم ۷۵ کیلوگرم وزن دارد.
انواع اورانیوم:
اورانیوم با غنای پایین که میزان اورانیوم ۲۳۵ آن کمتر از ۲۵% ولی بیشتر از۷/۰% است که سوخت بیشتر راکتورهای تجاری بین ۳ تا ۵ درصد اورانیوم ۲۳۵ است. اورانیوم با غنای بالا که در فرآیند غنیسازی اورانیوم تهیه میشود. اورانیوم ۲۳۵ در آن بیشتر از ۲۵% وحتی در مواردی تا ۹۸% است و مناسب برای کاربردهای نظامی وساخت بمبهای هستهای است.
منبع : مطالب ارسال شده
همچنین مشاهده کنید
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
خرید میز و صندلی اداری
خرید بلیط هواپیما
گیت کنترل تردد
ایران پاکستان مجلس شورای اسلامی رئیسی دولت رئیس جمهور سید ابراهیم رئیسی ایران و پاکستان حجاب مجلس دولت سیزدهم سپاه پاسداران انقلاب اسلامی
تهران سیل پلیس هواشناسی بارش باران فراجا شهرداری تهران فضای مجازی وزارت بهداشت سلامت قتل سازمان هواشناسی
بانک مرکزی خودرو قیمت خودرو ایران خودرو قیمت طلا قیمت دلار بازار خودرو دلار سایپا بورس تورم ارز
کتاب تلویزیون رادیو سینمای ایران سریال مهران مدیری نمایشگاه کتاب سینما فیلم تئاتر معماری فیلم سینمایی
کنکور ۱۴۰۳ دانشجویان دانشگاه آزاد اسلامی دانش بنیان بنیاد ملی نخبگان
رژیم صهیونیستی اسرائیل غزه آمریکا روسیه فلسطین جنگ غزه چین اتحادیه اروپا ترکیه عملیات وعده صادق اوکراین
فوتبال پرسپولیس استقلال باشگاه پرسپولیس اوسمار ویرا باشگاه استقلال رئال مادرید بارسلونا بازی سپاهان فوتسال لیگ برتر
گوگل همراه اول ایلان ماسک اپل شیائومی مایکروسافت هوش مصنوعی تبلیغات فناوری تلگرام سامسونگ ناسا
افسردگی یبوست پیری صبحانه