پنجشنبه, ۱۳ اردیبهشت, ۱۴۰۳ / 2 May, 2024
مجله ویستا
جفت الکترون پیوندی
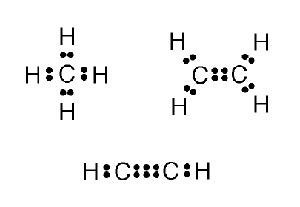
نقطهها ، جفت الکترونهای پیوندی را نشان میدهند.
● انواع جفت الکترون
▪ جفت الکترون ناپیوندی
جفت الکترون ناپیوندی ، جفت الکترونی است که در تشکیل پیوند کووالانسی شرکت ندارد و به شکل جفت الکترون تنها بر روی اتم قرار میگیرد و چون جفت الکترونهای ناپیوندی بیشتر تحت تاثیر یک هسته قرار میگیرند، تحرک بیشتری دارند و فضای بزرگتری اشغال میکنند. این جفت الکترونها در تشکیل پیوند هیدروژنی ، پیوند داتیو و تعیین شکل هندسی مولکول نقش اساسی دارند.
▪ جفت الکترون پیوندی
آنچه اتمهای یک مولکول را به هم متصل نگه میدارد، پیوند کووالانسی است. در تشکیل پیوند کووالانسی ، الکترونها به جای آنکه از اتمی به اتم دیگر منتقل شوند، میان دو اتم به اشتراک گذاشته میشوند. بعبارتی ، تمایل دو اتم برای از دست دادن یا گرفتن الکترون کم و بیش مشابه است. به همین دلیل ، بین آنها پیوند اشتراکی صورت میگیرد. در نتیجه ، جفت الکترونی که از اشتراک دو اتم در تشکیل پیوند کووالانسی حاصل میشود، به جفت الکترون پیوندی معروف است.
استحکام پیوند کووالانسی ناشی از کشش متقابل دو هسته مثبت و ابر منفی جفت الکترونهای پیوندی است یا به عبارت دیگر مربوط به آن است که هر دو هسته الکترونهای مشترک را جذب میکنند.
● نحوه تشکیل پیوند کووالانسی (جفت الکترونهای پیوندی)
برای ایجاد یک پیوند کووالانسی ، دو اتم بایستی به نحوی قرار گیرند که اوربیتال یکی از آنها قادر به همپوشانی با اوربیتال اتم دیگر باشد و هر اوربیتال باید دارای یک الکترون منفرد باشد. وقتی چنین شرایطی ایجاد شد، دو اوربیتال اتمی ، یک اوربیتال پیوندی منفرد را تشکیل میدهند که با هر دوا لکترون اشغال میشود.
دو الکترون مشترکی که یک اوربیتال پیوندی را اشغال مینمایند، بایستی دارای اسپین مخالف بوده ، یعنی بایستی زوج شده باشند. هر الکترون ، کل اوربیتال پیوندی را در اختیار دارد و بنابراین میتوان فرض کرد که به هر دو هسته اتمی متعلق است. آن آرایش الکترونها و هستهها ، حاوی انرژی کمتر یعنی پایدارتر از آرایش اتمهای مجزا است. در نتیجه ، تشکیل پیوند با آزاد شدن انرژی همراه است.
● پیش بینی تعداد جفت الکترونهای پیوندی برای یک اتم
اغلب میتوان تعداد پیوندهای جفت الکترونی را که یک اتم در یک مولکول بوجود میآورد، از تعداد الکترونهای مورد نیاز برای پر شدن پوسته والانس آن اتم (قاعده هشت تایی یا اُکتت) ، پیش بینی کرد.
چون برای عناصر اصلی جدول تناوبی ، شماره گروه با تعداد الکترونهای والانس برابر است، میتوان پیش بینی کرد که عناصر گروه هفت اصلی یعنی هالوژنها مثل کلر با هفت الکترون والانس برای رسیدن به هشت تایی پایدار یک پیوند کووالانسی ، عناصر گروه شش اصلی مثل S و O (با شش الکترون والانس) دو پیوند کووالانسی ، عناصر گروه پنج اصلی مثل P و N (با پنج الکترون والانس) سه پیوند کووالانسی و عناصر گروه چهار اصلی مثل C با چهار الکترون والانس چهار پیوند کووالانسی بوجود خواهند آورد.
هر اتم به تعداد الکترونهای جفت نشده خود پیوند کووالانسی تشکیل میدهد و اگر آرایش الکترونی عناصر گروه (۸-۳) اصلی جدول تناوبی را که میتوانند در پیوند کووالانسی شرکت کنند در نظر بگیرید، متوجه خواهید شد که اوربیتال نیمهپُر به اندازه کافی ندارند و یا انتظار دارید که Be و B نتوانند پیوند کوالانسی تشکیل دهند. در حالیکه مولکولهای گازی BeCl۲ با ساختار خطی و زاویه پیوندی ۱۸۰ درجه و BCl۳ با ساختار مثلثی و زاویه پیوندی ۱۲۰ درجه وجود دارند که بیانگر این مطلب است که Be دارای دو اوربیتال تک الکترونی و B دارای سه اوربیتال تک الکترونی بوده و در پیوند کووالانسی با اتم کلر شرکت نمودهاند.
● برانگیخته شدن برای تولید الکترونهای منفرد
اگر در حالت اصلی ، اتمی اوربیتال نیمهپر کافی نداشته باشد، با استفاده از حالت برانگیخته (ارتقای الکترون) تعداد کافی اوربیتال نیمه پر پیدا میکند. حالت برانگیخته برای بسیاری از اتمها برای تشکیل پیوند کووالانسی صورت میگیرد و این ارتقای الکترون ، باید از یک لایه فرعی دیگر (در همان لایه اصلی) باشد. مثلا از ۲s به ۲p یا از ۳s به ۳p یا به ۳d.برای مثال ، اتم کربن در حالت اصلی (حالت پایه) ۲ الکترون منفرد دارد، در صورتی که در ترکیبهای مختلف ، کربن چهار ظرفیتی است، یعنی ۴ الکترون با اتم دیگر به اشتراک میگذارد و ۴ زوج الکترون مشترک تشکیل میدهد. بنابراین به صورت زیر برانگیخته میشود:
۱s۲ ۲s۲ ۲p۲(energy) →۱s۲ ۲s۱ ۲p۳
ارتقای الکترون در اتم کربن به صورت ۲s۱ ۲p۲ به ۴۰۶ کیلوژول انرژی نیاز دارد. در نتیجه ، اوربیتال هیبریدی sp۳ (یک s وسه p) تشکیل میدهد.
● مولکول IF۳
در مولکول IF۳ نیز اتم یُد باید ۳ الکترون منفرد داشته باشد، بنابراین باید برانگیخته شود و یک الکترون از لایه ۵p به لایه ۵d انتقال یابد. لایه ظرفیت یا والانس اتم یُد بصورت ۵s۲ ۵p۵ میباشد که درحالت برانگیخته بصورت ۵s۲ ۵p۴ ۵d۱ در میآید و در نتیجه سه الکترون منفرد حاصل میشود که با سه اتم فلوئور پیوند کووالانسی تشکیل میدهند.
● مولکول BeCl۲
اتم بریلیم دارای ۲ الکترون جفت شده در اوربیتال ۲s میباشد که یکی از الکترونها در اثر برانگیخته شدن به اوبیتال ۲p انتقال مییابد و دو اوربیتال هیبریدی sp حاصل میشود که با اتمهای کلر پیوند کووالانسی بوجود میآورد.
● مولکول BCl۳
اتم بور (B) در حالت پایه دارای ۲ الکترون در اوربیتال ۲s و یک الکتون در اوبیتال ۲p میباشد. برای تشکیل مولکول ، باید اتم B از حالت پایه ۱s۲ ۲s۲ به حالت برانگیخته ۱s۲ ۲s۱ ۲p۲ تبدیل شود و در اثر هیبرید شدن اوربیتالها ، سه اوربیتال هیبریدی sp۲ حاصل میشود که با اتمهای کلر ، پیوند کووالانسی تشکیل میدهند.
● خطوط ، جفت الکترونهای پیوندی را نشان میدهند.
▪ دو اتم میتوانند بیش از یک جفت الکترون به اشتراک بگذارند
از آن جا که کربن در بیرونیترین لایه الکترونی خود چهار الکترون ظرفیت دارد، با رعایت قاعده هشت تایی ، حداکثر میتواند با چهار اتم ، پیوند تشکیل دهد. در مولکول اتان ، C۲H۶ ، هر اتم کربن به یک کربن و سه اتم هیدروژن متصل است. بین هر اتم هیدروژن و کربن و همچنین بین دو اتم کربن ، یک جفت الکترون مشترک وجود دارد. اما در مولکول اتن ، C۲H۴ ، بین دو اتم کربن دو جفت الکترون مشترک وجود دارد.
افزون بر کربن ، عنصرهای دیگر از جمله نیتروژن ، اکسیژن و گاهی گوگرد نیز میتوانند با اتمهای دیگر ، با رعایت قاعده هشتتایی ، بیش از یک جفت الکترون به اشتراک بگذارند. اگر بین دو اتم به جای یک جفت الکترون ، دو جفت الکترون به اشتراک گذاشته شود، یک پیوند کووالانسی دو گانه یا پیوند دوگانه تشکیل میشود و همچنین اگر بین دو اتم به جای یک جفت الکترون ، سه جفت الکترون به اشتراک گذاشته شود، پیوند سه گانه تشکیل میشود. مانند مولکول نیتروژن ( N۳ ) که در آن بین دو اتم نیتروژن ، سه جفت الکترون پیوندی وجود دارد.
حامد حاتمی
http://chemtown.blogfa.com
http://chemtown.blogfa.com
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
خرید بلیط هواپیما
ایران دولت نیکا شاکرمی روز معلم معلمان رهبر انقلاب مجلس شورای اسلامی مجلس دولت سیزدهم حجاب شهید مطهری شورای نگهبان
تهران زلزله هواشناسی معلم شهرداری تهران سیل قوه قضاییه آموزش و پرورش پلیس سلامت سازمان هواشناسی دستگیری
خودرو قیمت خودرو بانک مرکزی قیمت دلار دلار ایران خودرو قیمت طلا سایپا کارگران بازار خودرو تورم قیمت
مسعود اسکویی فضای مجازی تلویزیون رضا عطاران سریال سینمای ایران سینما دفاع مقدس موسیقی تئاتر
دانشگاه علوم پزشکی مکزیک
رژیم صهیونیستی غزه اسرائیل فلسطین آمریکا جنگ غزه چین روسیه نوار غزه حماس عربستان ترکیه
استقلال پرسپولیس فوتبال سپاهان تراکتور لیگ برتر ایران رئال مادرید بایرن مونیخ باشگاه استقلال لیگ قهرمانان اروپا لیگ برتر باشگاه پرسپولیس
اینستاگرام همراه اول دبی واکسن اپل ناسا وزیر ارتباطات تبلیغات گوگل پهپاد
کبد چرب بیماری قلبی کاهش وزن دیابت داروخانه ویتامین طول عمر بارداری