جمعه, ۱۴ اردیبهشت, ۱۴۰۳ / 3 May, 2024
مجله ویستا
خونی به رنگ سرطان
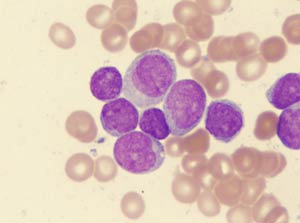
● سیر تکاملی درمان
به دنبال شناخت بیماری لوسمی میلوژنوس مزمن و آشنایی با اصول بیماری، استفاده از درمانهای دارویی برای کنترل آن متداول شد. «محلول فولر» (Fowler)، آرسنیکتریاکساید حل شده در کربنات پتاسیم است که در سال ۱۸۷۸ برای درمان لوسمی میلوژنوس مزمن به کار گرفته شد. وقتی که این محلول به بیمار مبتلا برای مدت ۱۰ هفته داده شد، لوکوسیتوز رو به کاهش رفت اما پس از قطع درمان، مجددا افزایش یافت. در نتیجه «محلول فولر» تا شروع قرن حاضر، درمان متداولی برای لوسمی میلوژنوس مزمن و سایر بدخیمیهای خونی بود.
اکتشاف «بوسولفان» (Busulfan) در سالهای ۱۹۵۰ گزینه درمانی دیگری بود. به طور روتین در ابتدا «بوسولفان» در دوزهای منقطع خوراکی با دوزاژ ۶ میلیگرم در روز تجویز میشود و بیماران در طول درمان از نظر کاهش لوکوسیتوز تحت بررسی قرار دارند. الگوی متناوب مصرف دارو با هدف کاهش علایم مسمومیت نظیر پیگمانتاسیون پوستی، فیبروز ریوی و اختلالات باروری طراحی شده بود. وقتی میزان گلبولهای خونی بیمار به کمتر از میزان مورد انتظار سقوط میکرد، دارو قطع میشد. همچنین هرگاه در بیماری تشخیص داده میشد که درمان متناوب بیاثر است، دوز ممتد دارو تجویز میشد. داروهای دیگری نظیر «۶-مرکاپتوپورین»، «اوراسیل موستارد» و «دیبرومومانیتول» هم مطرح بودند اما تجویز آنها به دلیل کم فایده بودنشان محدود شد.
در سالهای ۱۹۵۰ مشخص شد که «هیدروکسی اوره» اثرات ضد تومورال دارد، بنابراین بر ضد طیف وسیعی از بدخیمیها از جمله لوسمی میلوژنوس مزمن بهکار گرفته شد. در ۱۹۶۰ مطالعات متعدد نشان دادند که «هیدروکسی اوره» میتواند در کنترل لوکوسیتوز در مبتلایان به لوسمی که پس از درمان خط اول با «بوسولفان»، مجددا با عود روبهرو بودهاند، به کار رود. در ۱۹۷۲ مطالعات بالینی مطرح کرد که «هیدروکسی اوره» میتواند به عنوان خط اول درمانی تجویز شود. در مطالعهای که در سال ۱۹۸۲ منتشر شد، این نظریه مطرح گردید که تجویز «هیدروکسی اوره» با وجود اثربخشی یکسان در مقایسه با «بوسولفان»، میزان شانس بقای بیمار را افزایش میدهد.
در سالهای ۱۹۷۰، درمان لوسمی به سمت پیوند آلوژنیک سلول بنیادی گرایش یافت. هر چند که پیوند مغز استخوان، درمان دردسترسی برای مبتلایان به لوسمی است اما کاربرد این روش به دلیل محدودیت داوطلبان دهنده پیوند و عوارض درمان نظیر ابتلا به بیماریهای انسدادی وریدهای کبدی و عفونتهای کشنده، از رونق افتاد.
کم شدن گرایش به کاربرد پیوند مغز استخوان، به رواج سایر روشهای درمانی لوسمی از جمله طرح «اینترفرونآلفا» انجامید. اخیرا این دارو در درمان لوسمی میلوژنوس مزمن با دوزاژ ۳MU در روز برای سه روز و به دنبال آن افزایش دوز به ۶MU برای سه روز دیگر و سپس ادامه درمان با ۹MU به طور روزانه مورد تایید قرار گرفته است. شایعترین عوارض جانبی« اینترفرون آلفا» عبارتند از سندروم شبه فلو که با علایمی نظیر تب، خستگی، درد عضلانی، لرز، درد مفصل و سردرد خود را نشان میدهد. بیاشتهایی، افسردگی، تهوع، استفراغ و اسهال نیز در بعضی موارد دیده میشود. در اواسط دهه ۱۹۹۰ مشخص شد که افزودن «سیتارابین» در مقایسه با «اینترفرون-آلفا»، به تنهایی قابلیت بیشتری در افزایش طول عمر بیماران دارد.
● درمانگرهای جدید
«ایماتینیب» (گلیوک Gleevec) در فاز اول مطالعات بالینی مورد تایید قرار گرفت زیرا در بیماران مقاوم به درمان با اینترفرون آلفا، پاسخهای هماتولوژیک و سیتوژنیک بیشتری ایجاد کرد. همچنین «ایماتینیب» در بیمارانی که به درمان با «هیدروکسی اوره»، «بوسولفان» یا «اینترفرون» با«سیتارابین» پاسخ نداده بودند، سودمند بود. در واقع «ایماتینیب» انقلابی در درمان لوسمی میلوژنوس مزمن بر پا کرد اما به مرور، محدودیتهای طیف فعالیت آن مشخص شدند. هر چند که بیماران مبتلا به این بیماری، پاسخ قابل قبولی به «ایماتینیب» دادند، اما عود بیماری گزارش شده است. «دازاتینیب» با نام تجاری اسپریسل (Sprycel) در سال ۲۰۰۶ از سوی FDA برای درمان لوسمی میلوسیتیک مزمن و لوسمی لنفوسیتیک حاد با کروموزوم فیلادلفیای مثبت مورد تایید قرار گرفت. ارزیابی بالینی «دازاتینیب» روی بیمارانی که پس از پاسخ درمانی، عود داشتهاند یا به دلیل عوارض جانبی نتوانسته بودند دارو را تحمل کنند، ترتیب داده شد. ۴۴ درصد از بیماران پاسخ درمانی هماتولوژیک کامل و ۲۱ درصدشان پاسخ سیتوژونیک قابل توجهی بروز داده بودند. «دازاتینیب» به شکل قرصهای خوراکی موجود است. مقادیر ۲۰، ۵۰ و ۷۰ میلیگرم به شکل قرص تعبیه شدهاند.
«نیلوتینیب»، مهارکننده انتخابی تیروزین کیناز است که اخیرا تولید شده است. البته مطالعات بالینی کاملتری برای اثبات تحملپذیری و بیخطر بودن و نیز فعالیت ضد لوسمی آن لازم است. به هر حال به نظر میرسد که «نیلوتینیب» نیز مشابه «دازاتینیب» خط دوم درمان در بیمارانی باشد که به دنبال درمان با «ایماتینیب» عود داشتهاند یا نتوانستهاند درمان اولیه با این دارو را تحمل کنند.
منبع : هفته نامه سپید
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
تعمیر جک پارکینگ
خرید بلیط هواپیما
ایران تهران انتخابات عراق دانشگاه تهران رهبر انقلاب مجلس شورای اسلامی دولت دولت سیزدهم روز معلم نیکا شاکرمی مجلس
سیل آتش سوزی هواشناسی شهرداری تهران آموزش و پرورش یسنا پلیس قوه قضاییه فضای مجازی معلم زلزله سلامت
قیمت خودرو تورم سهام عدالت قیمت طلا سازمان هواشناسی خودرو بازار خودرو قیمت دلار قیمت سکه ایران خودرو بانک مرکزی حقوق بازنشستگان
مهران غفوریان ساواک موسیقی تلویزیون سریال عمو پورنگ سینمای ایران تبلیغات نمایشگاه کتاب مسعود اسکویی عفاف و حجاب سینما
رژیم صهیونیستی فلسطین اسرائیل غزه آمریکا جنگ غزه روسیه ترکیه حماس انگلیس نوار غزه اوکراین
استقلال فوتبال پرسپولیس سپاهان آتیلا حجازی باشگاه استقلال علی خطیر لیگ برتر بازی لیگ برتر ایران تراکتور رئال مادرید
اپل هوش مصنوعی فناوری آیفون گوگل ناسا مدیران خودرو تلفن همراه
خواب طب سنتی کبد چرب فشار خون بیماری قلبی